Capitulo 2 - Noções de Física Nuclear
Dimensões Nucleares
| A experiência de Rutherford originou o modelo atômico mencionado no início deste capítulo, e que foi sistematizado por Bohr (trataremos disso no cap. 4). O modelo anterior, proposto por Thomson, consistia numa mistura homogênea de prótons e elétrons. Esse modelo passou a ser conhecido como modelo do pudim de ameixa. Os prótons representavam o pudim, e os elétrons eram as ameixas. | 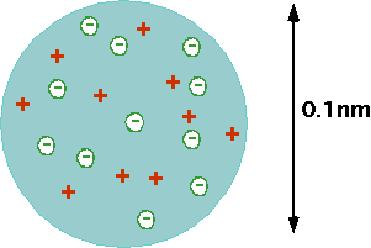 |
Entre 1908 e 1911, Rutherford fez os experimentos que hoje conhecemos como espalhamento de Rutherford. Ele lançou partículas alfa contra folhas finíssimas de vários metais pesados, incluindo ouro, e observou resultados muito estranhos, conforme ilustra a animação abaixo.
Várias partículas eram espalhadas em ângulos enormes, e algumas eram até espalhadas para trás. Por tudo que se sabia da teoria eletromagnética, e se o modelo de Thomson fosse verdadeiro, os desvios das partículas a deveriam ser bem menores, como na animação abaixo.
A partir do espalhamento desssas partículas, Rutherford estimou o raio nuclear, considerando que este é aproximadamente igual à distância mais próxima ao núcleo, atingida pela partícula a. Vejamos como se faz este cálculo.
A partícula tem energia cinética Ec=7.7 Mev. Quando esta partícula é lançada frontalmente contra o núcleo, a interação Coulombiana faz com que sua energia cinética seja transformada em energia potencial eletrostática. Quando toda a energia cinética é transformada em energia potencial, a partícula chega à distância mais próxima, e pára. Nesse momento,
Utilizando os valores numéricos conhecidos (1/4pe0 =9x109 Nm/C2; e=1.6x10-19 C), obtém-se
Portanto, o raio do núcleo de ouro deve ser menor do que 3x10-14 m, isto é, menos do que 1/10000 do raio atômico. É razoável esperar que o volume nuclear seja proporcional ao número de massa. Assim, considerando o núcleo como uma esfera de raio R, tem-se
Para o ouro, A=197, tem-se R=7x10-15m. Com esta dimensão, resulta que a densidade da matéria nuclear é da ordem de 2x1017 kg/m3.
As dimensões nucleares são mais convenientemente descritas através de uma nova unidade, denominada fermi ou fentômetro (fm), definida por 1 fm = 10-15 m.
| |
|
|